Российские химики создали батарею, которая может работать на химических отходах
Исследователи из РХТУ им. Д.И. Менделеева, ИПХФ РАН и ИФХЭ РАН разработали нейтрализационную батарею — устройство, способное генерировать электричество за счет разности рН двух жидкостей. Например, в ней можно использовать стоки отработанных кислот и щелочей с химических производств.
Конструкцию нейтрализационной батареи отработали на разбавленных растворах HCl и NaOH. Была показана принципиальная возможность перезаряда устройства, а ее удельная мощность достигала более 6 мВт/см2 — это один из самых высоких показателй среди всех нейтрализационных батарей. Результаты исследования опубликованы в журнале ChemSusChem.
С каждым годом в мире производят все больше электричества и людям нужно всё больше накопителей энергии. Они бывают разного типа — от привычных литий-ионных аккумуляторов и свинцово-кислотных батарей до водородных топливных элементов и многих других. У каждой технологии свои плюсы и минусы: какие-то накопители почти не разряжаются в режиме простоя и поэтому подходят для долгосрочного хранения электричества, другие могут выдавать очень большие токи, а третьи — хранить рекордное количество энергии в пересчете на единицу своей массы, что делает их незаменимыми, например, для подводных лодок.
Среди накопителей энергии бывают и особенно экзотические. Так, в 70-х годах XX века ученые предложили концепцию нейтрализационной батареи, в которой энергия получается за счет разницы в значениях рН двух жидкостей, называемых электролитами. Фактически это топливо, которое превращается в электричество. Нейтрализационные батареи обладают достаточно низкими характеристиками: они не дают большие мощности при разряде и не могут хранить большие объемы энергии, но зато у них есть важное преимущество — стоимость электролитов. Для литий-ионных аккумуляторов нужны сравнительно дорогие соли лития, для водородных топливных элементов нужен водород, а нейтрализационные батареи могут использовать практически любые жидкости – например, стоки отработанных кислот и щелочей с химических производств или даже морскую воду.
“Если взять какую-нибудь кислоту и щелочь – например, банальные гидроксид натрия NaOH и соляную кислоту HCl — и слить их вместе, то у нас самопроизвольно пойдет реакция нейтрализации. Из NaOH и HCl образуется соль NaCl, а оставшиеся —ОН и —H сольются в воду — H2O. Суммарная энергия, запасенная в химических связях NaCl и H2O, ниже, чем суммарная энергия исходной кислоты и щелочи, и поэтому в этой реакции появляется избыток энергии, который рассеивается вместе с теплом. Проще говоря, стакан, в котором мы смешали исходные реагенты, нагревается, — рассказывает сотрудник лаборатории ЭМХИТ РХТУ и первый автор работы Павел Локтионов. — В нейтрализационной батарее мы проводим точно ту же реакцию, но только разбиваем ее на две полуреакции и разносим их в пространстве. На одном электроде протекает одна полуреакция, на другом другая, а в сумме они дают ту же самую реакцию нейтрализации, но только энергия здесь выделяется не в виде тепла, а в виде электронов, которые образуются в одной полуреакции и потребляются в другой. Поначалу эта идея кажется каким-то трюком, уловкой, в которой электричество получается почти из ничего, но потом видишь, что батарея работает: она запасает и высвобождает электричество в полном соответствии с формулами и здравым смыслом”.
Круговорот веществ в батарее
Существуют разные конструкции нейтрализационной батареи, но всех их объединяет общая идея — две жидкости с отличным рН прокачиваются через разные емкости внутри батареи. Они физически не смешиваются между собой, но зато вступают в электрохимические реакции, некоторые продукты которых переходят из одной емкости в другую. За счет такого своеобразного круговорота веществ и выделяется или, наоборот, запасается энергия. Ключевая идея батареи российских ученых — это использование двух водородных электродов, то есть в обеих емкостях происходят реакции с участием водорода, и суммарная реакция нейтрализации составляется именно из них.
Сама разработанная ячейка была разделена на три части. В левую, прикатодную часть непрерывно подавался HCl, который диссоциировал на протоны H+ и хлорид-анионы Cl-, а в правую, прианодную — NaOH, который, в свою очередь, диссоциировал на Na+ и OH+. При разряде батареи на катоде ионы H+ превращались в H2. Дальше водород передавался в правую треть батареи, где уже встречался с OH- на аноде и превращался в воду.
Получается, что поток водорода в этой системе закольцован — при заряде он выделяется слева на катоде и потребляется справа на аноде. Точно так же закольцован и поток электронов — они, наоборот, выделяются справа на аноде, уходят во внешнюю цепь, там совершают полезную работу, а потом приходят на катод, чтобы поучаствовать в реакции восстановления H+. Наконец, в третью часть батареи — ту, которая на схеме расположена посередине, — приходят ионы Na+ и Cl-, образовавшиеся при диссоциации кислоты и щелочи. Там Na+ и Cl- объединяются в соль NaCl, как и должно быть в реакции нейтрализации. При этом все эти реакции и потоки можно обратить в строго обратную сторону — тогда батарея будет не разряжаться, а заряжаться.
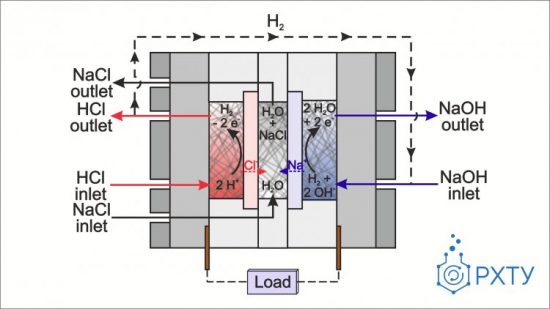
Схематическое изображение основных принципов работы нейтрализационной батареи. Изображение предоставлено авторами исследования
В своей работе ученые оценили, как на характеристики новой нейтрализационной батареи влияет концентрация используемых кислоты и щелочи, а также структура каталитической поверхности электродов, на которых и протекают нужные окислительно-восстановительные реакции. Они показали, что эффективность работы батареи сейчас определяется в основном реакцией окисления водорода, протекающей на аноде. И после оптимизации всех условий у них получилась батарея с удельной мощностью до 6.1 мВт/см2 и плотностью хранимой энергии до 7.4 Вт-ч/л.
Как разглядеть атомную электростанцию в химических стоках?
“По сравнению с другими накопителями энергии у нас получились скромные показатели – например, те же литий-ионные аккумуляторы дают плотность энергии где-то до 600 Вт-ч/л, – рассказывает Павел Локтионов. – Но среди именно нейтрализационных батарей мы, наоборот, получили очень неплохие цифры, а теперь стараемся их улучшить. Так, плотность хранимой энергии можно поднять в разы за счет увеличения концентрации электролитов — мы использовали растворы кислоты и щелочи концентрацией 1 моль на литр, хотя их предельная растворимость гораздо больше. А удельную мощность можно заметно повысить, если еще поработать с электродными поверхностями. После таких доработок нейтрализационная батарея вполне может найти свою нишевую область применений”.
Так, по оценкам некоторых исследователей, если в качестве кислых электролитов нейтрализационных батарей просто использовать стоки, которые образуются при производстве серной и фосфорной кислот, то суммарно будет получаться 1100 ГВт-ч энергии в год. Для сравнения: все атомные электростанции России вырабатывают ежегодно около 200 ГВт-ч энергии. При этом важно не забывать, что нейтрализационная батарея — это вторичный источник тока, то есть она может не только разряжаться, необратимо “сжигая” топливо, но еще и потом обратно заряжаться.
Пока российские ученые подчеркивают, что их исследование — это только принципиальная демонстрация работоспособности новой конструкции нейтрализационной батареи с двумя водородными электродами, сделанная на разбавленных растворах HCl и NaOH. Но в перспективе такая нейтрализационная батарея, конечно, может использовать и более концентрированные растворы или вообще другие электролиты. Сейчас исследователи дорабатывают конструкцию своей нейтрализационной батареи и готовят патент на разработку.
Источник: scientificrussia.ru
________________________________________________________________________________
BATTERY-INDUSTRY.RU ВКонтакте
BATTERY-INDUSTRY.RU в Telegram

















